| أزيد صوديوم | |
|---|---|
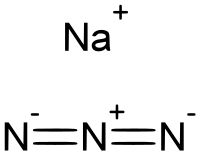 |
|
| معلومات عامة | |
| الاسم النظامي | أزيد صوديوم |
| أسماء أخرى | ثلاثي نتريد صوديوم |
| الصيغة الجزيئية | NaN3 |
| رقم CAS | [26628-22-8] |
| خواص | |
| الكتلة المولية | 65.02 غ/مول |
| المظهر | مسحوق بلوري أبيض |
| الكثافة | 1.85 غ/سم3 |
| الانحلالية في الماء | 41.7 غ/100 مل (عند 17°س) |
| درجة الانصهار | 275 °س |
| درجة الغليان | >300 °س يتفكك |
| في حال عدم ذكر الشروط فإن
البيانات الواردة أعلاه مقاسة في الشروط النظامية ومدونة حسب النظام الدولي للوحدات |
|
أزيد الصوديوم هو مركب كيميائي له الصيغة NaN3، ويكون على شكل مسحوق بلوري أبيض، ينحل بالماء بشكل جيد، لكنه بالكاد ينحل بالإيثانول، وهو غير منحل في ثنائي إيثيل الإيثر، ومحاليله في الماء قلوية.
فهرس
|
التحضير
يتم الحصول على أزيد الصوديوم بمردود جيد من تفاعل أميد الصوديوم مع غاز الضحك (أكسيد النتروس).
+
الخواص
يتفكك أزيد الصوديوم عند درجات حرارة أعلى من 300°س إلى الصوديوم وغاز النيتروجين حسب المعادلة:
وعلى أساس هذا التفاعل يعتمد عمل الوسائد الهوائية (Airbags) في السيارات (انظر ← الاستخدامات)
الاستخدامات
- له تطبيق مهم في الوسائد الهوائية للسيارات.
يعتمد عمل الوسادة الهوائية من وجهة نظر كيميائية على ثلاثة مكونات رئيسية
- أزيد الصوديوم NaN3
- نيترات البوتاسيوم KNO3
- ثنائي أكسيد السيليكون SiO2
لحظة حدوث التصادم يتم إشعال أزيد الصوديوم كهربائياً حيث يتقكك بشكل متفجر مولداً غاز النيتروجين خلال ما يقارب 40 ميلي ثانية فيملأ بالتالي كيس البولي أميد فينتفخ بسرعة.
أكثر من ذلك فإن الصوديوم الناتج يتفاعل مع نيترات البوتاسيوم المتواجدة في الكيس فيعطي أكسيد الصوديوم وأكسيد البوتاسيوم بالإضافة إلى كمية أخرى من غاز النيتروجين
أكسيدا المعدنين القلويين يتفاعلان بالنهاية مع أكسيد السيليكون ليعطي السيليكات الموافقة.
المصادر
Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4