فهرس |
الأحماض الكربوكسيلية
نبذة عامة
- • الأحماض الكربوكسيلية هي أحماض عضوية تصنف في ظل وجود مجموعة الكربوكسيل الفعالة COOH)).
- • كما أنها تندرج تحت تصنيف العالمين (برونشتد ولاوري) للأحماض ، حيث تقوم بمنح البروتون.
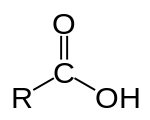
- • صيغتها العامة هي R-COOH.
- • حيث R من الممكن أن تكون إما جذر ألكيلي أو ذرة هيدروجين.
- • وهي منتشرة في الطبيعة بشكل كبيـر.
الصفات الفيزيائية
- • الأحماض الكربوكسيلية هي مـركبات قطبية ، بالتالي بإمكانها تكوين روابط هيدروجينية بين الجزيئات.
- • في درجات الحرارة المرتفعة ، تتواجد الأحماض الكربوكسيلة على شكل مركب مزدوج الصيغة الجـزيئـيةDimeric pairs.
- • الأحمـاض الكربـوكسـيلية ذات الحجـم الصغيـر ( 1 - 4 ذرات كربون ) لها قـابـلية الـذوبان في المــاء.
- • بينما ذوات الحجم الأكبر ( 5 ذرات فأكثر ) تقل قابلية الذوبان لديها ، وهذا يعود إلى ازدياد عدد ذرات الكربون في المركب.
- • حيث من المعلوم ان ذرات الكربون كارهة للماء (Hydrophobic). لذلك هي ميالة أكثر لأن تذوب في المحاليل الأقل قطبية كالإيـثرات والكـحول.
- • فعليا ً ، تعتبر هذه المركبات أحماضا ً ضعيفة ، أي أنها تتفكك وتتحلل جزئيا ً لتعطي H+ وRCOO− في المحاليل المائية.
استقرارية الحمض
- • إذا تمعنا في التأثير الحثي Inductive effect)) ، نجد أن تفسير حمضية الأحماض الكربوكسيلية يعود إلى ذرة الأكسجين ذات السالبية الكهربائية.
- • والتي بدورها تقوم بتدمير السحابة الإلكترونية المحيطة على الرابطة O-H وبالتالي إضعافها.
- • هذي الرابطة الضعيفة تجعل الجزيء أقل استقرارا ً ، كما تجعل ذرة الهيدروجين أقل استقرار وثباتية.
- • فبالتالي يسهل تـفـفكها ليعطينا بروتونا ً موجبا ً H+ . ( تعريف برونشتد ولاوري للمركبات الحمضية ).
- • وبما أن الحمض غير مستقر ، هذا سيؤدي إلى أن التوازن سيتجه لجهة اليمين أكثر.
- • في حال إضافة ذرات أو مجموعات ذات سالبية كهربائية عالية للمركب مثل الكلور وذرة الهـيدروكسيل ، تزيد من الحامضية بالتأثير الحثي.
- • على سبيل المثال ، ثلاثي كلورو حمض الخل ( 3 ذرات كلور ) أقوى حامضية من حمض اللبن ( ذرة هيدروكسيل واحدة ) ، والذي بدوره يعتبر أقوى حامضية من حمض الخل ( لا يحتوي على إضافات ) .
استقرارية القاعدة المقترنة
- • يمكن تفسير حمضية الأحماض الكربوكسيلية عن طريق التـأثـيـر الـرنيني (resonance effect) .
- • فبعد تفكك الحمض الكربوكسيلي ينتج مركب ذات تأثير رنيـــني ثابت.
- • بحيث يتم التشارك بالإشارة السالبة بين ذرتي الأكسجيــن.
- • ويتواجد في الرابطة بين الكربون والأكسجين ما يعرف بـ ( خصائص الرابطة المزدوجة ).
- • فبما أن القاعدة المقترنة مستقرة ، إذن فإن سهم التوازن الأعلى يميل إلى جهة اليمين من التفاعل.
طرق تحضير وتصنيع هذه المركبات
يمكن تحضير هذه المركبات بعدة طرق... منها:
- • أكسدة الكحول الأولية مع الألدهيدات بمؤكسدات قوية. مثل ( كاشف تولن ، بريمنجنات البوتاسيوم ).
- • الأكسدة الكلية لذرة ألكيل مرتبطة مع حلقة بنزين. وذلك بغض النظر عن طول سلسلة ذرة الألكيل.
- • تميؤ الإسترات أو الأميدات أو النيترات بإضافة قاعدة أو حمض.
- • تفاعل كاشف جرينيارد مع ثاني أكسيد الكربون ( على الرغم من عدم انتشار هذه الطريقة تجاريا ً ).
تفاعلاتها
هنا نذكر البعض من تفاعلات الأحماض الكربوكسيلية.
- • تتفاعل الأحماض الكربوكسيلية مع القواعد لتكون أملاح الحمض. بحيث يتم استبدال ذرة الهيدروجين المتواجدة على الرابطة O-H بمعدن.
CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
- • كما تتفاعل مع الكحول والأمينات لتنتج الإسترات والأميدات.
- • تفاعلات آرندت إيستيرت ، حيث يتم إدخال مجموعة α – ميثيلين للحمض الكاربوكسيلي.
- • تفاعلات إعادة ترتيب كورتيس ، تحول الحمض الكاربوكسيلي إلى أيزو سيانيت.
- • تفاعلات شميديت ، تحول الأحماض الكربوكسيلية إلى أمينات.
- • في تفاعلات هندسديكر ، يتم انتزاع ذرة كربوكسيل.
- • تفاعلات ديكون ويست ، تحول الأحماض الأمينية إلى كيتون أمين مماثــل.