الامتصاص والتكثيف ( Absorption and adsorption )
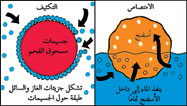 |
كيف يختلف الامتصاص عن التكثيف |
الامتصاص:
هنالك كثير من الأمثلة المألوفة للامتصاص. فالستائر الثقيلة تمتص الطاقة الصوتية. تجعل الموجات الصوتية خيوط الستائر تتذبذب وتحتك بعضها ببعضها الآخر. ويحوِّل الاحتكاك طاقة الصوت إلى حرارة، لذا فإن الصوت لايمكنه أن ينعكس مثل الصدى. ★ تَصَفح: العزل. تمتص الأجسام الملونة والمرشحات طاقة الضوء انتخابيًا. ويتكون الضوء الأبيض من كل ألوان الضوء. وحين يلامس الضوء الأبيض جسمًا ملونًا فإنّ بعض ألوان طاقة الضوء يتم امتصاصها. وتثير طاقة الضوء الممتصَّة الإلكترونات داخل ذرات الجسم الملوّن ـ بمعنى أنها تُنَشِّطها إلى مستويات عليا من الطاقة. ويقوم الجسم بإرسال أو عكس ألوان الضوء الذي لم يتمّ امتصاصه. وتمتص التربة اليابسة الماء عن طريق الخاصيَّة الشِعرية. ★ تَصَفح: الخاصية الشعرية. يمتص الماء في البحيرة الأكسجين بالإذابة.التكثيف:
المادة الصلبة هي وحدها التي يمكنها دائمًا أن تكون مكثِّفًا. المادة المكثَّفة قد تكون جزيئات سائل أو غاز أو جسيمات دقيقة لجسم صلب. وعادة مايكون التكثيف انتخابيا بدرجة عالية مما يفيد في فصل أو تنقية السوائل والغازات. يُكثِّف المرشح الفحمي على سطح كل جسيم فحمي. ويكثف هلام السليكا (ثاني أكسيد السليكيون) جزيئات الماء من رطوبة، ويحفظها على سطح كل حبّة. ويطلق التكثيف حرارة تُسميَّ حرارة التكثيف.ويكون تفاعل الجزيئات المكثَّفة مع السطح المكثِّف قويًا أو ضعيفًا. وتكون الجزيئات ضعيفة الارتباط عندما تكون قوة الجذب بينها وبين السطح المكثف فيزيائيًا. وتسمى هذه العملية الامتصاص الفيزيائي.
وحين تتحد الجزيئات المكثَّفَة كيميائيا مع السطح فإنها تلتصق به بشدة. وتسمى هذه العمليّة بالامتصاص الكيميائي. تكوّن الجزيئات المكثفة في الامتصاص الكيميائي طبقة واحدة ؛ لكنها ربما تكوِّن عدة طبقات في عملية الامتصاص الفيزيائي.
★ تَصَفح أيضًا: النبات.
المصدر: الموسوعة العربية العالمية